Статья поступила в редакцию 14.01.2020 г.
УДК 567.8
© 2020 г. Книсс В.А.*, Морозова И.М.**, Морозов М.К.**
*Институт экологической экспертизы и биоинформационных технологий.
Респ. Башкортостан, Уфимский район, 450571, д. Юматово, ул. Парковая, д. 36.
**Башкирское отделение Московского общества испытателей природы.
Респ. Башкортостан, Уфимский район, 450571, д. Юматово, ул. Парковая, д. 36.
// Материалы по флоре и фауне Республики Башкортостан. 2020. № 26. С. 20-28.
Влияние выделяемых лягушками содержащихся в кожной слизи веществ на деятельность молочнокислых бактерий заметили ещё в древности. Однако более детально изучать эту проблему начали лишь с середины 1970-х годов.
В настоящее время в научно-исследовательских лабораториях многих стран ведутся разработки лекарственных средств на основе выделяемых амфибиями соединений-пептидов как аналога антибиотиков, позволяющих бороться с бактериями, вирусами и грибками (Nascimento et al., 2003). В частности, результаты таких исследований показали, что антимикробные пептиды настоящих лягушек полезны, прежде всего, как вещества, активно подавляющие различные инфекции (Ponti et al., 2003). На сегодняшний день известна противораковая, иммуномодулирующая и антимикробная активность таких пептидов. Кроме того, экзометаболиты могут использоваться и в фармацевтике, прежде всего, за счёт своей избирательности по отношению к разнообразным патогенам. Вполне возможно использовать их в сельскохозяйственном производстве и пищевой промышленности.
Так, в 2016 г. Т.Х. Тимохиной с соавторами в Тюменском медицинском университете было впервые проведено комплексное изучение влияния состава корневых экзометаболитов пшеницы на рост, колонизацию и антигрибковую активность ризобактерий в условиях, моделирующих ризосферу отдельных растений. Установлено, что наибольшей бактерицидной активностью в отношении тест-штамма золотистого стафилококка St. aureus обладали двухсуточные экзометаболиты. При этом была отмечена массовая гибель St. aureus через 30 мин. экспозиции совместно с экзометаболитами бактерии B. bifidum (Тимохина, 2016). Результаты данной работы можно использовать и для более результативного применения ризобактерий, стимулирующих рост растений (PGPR – plant growth promoting rhizobacteria) в сельскохозяйственной практике. С целью повышения эффективности ассоциативного симбиоза PGPR с другими (не бобовыми) растениями, с одной стороны, при селекции бактерий целесообразно учитывать их способность утилизировать основные компоненты корневых выделений, которая может определять уровень ассоциативности бактерий с растением. С другой стороны, соотношение органических кислот к сахарам в корневых выделениях является признаком, по которому можно вести селекцию растений.
Результаты эксперимента, проведённого В.А. Валуевым (2013) показывают, что полученный им раствор экзометаболитов, разбавленный в 10 тыс. раз оживляюще действует на подвергнутые слабому отравлению зёрна пшеницы. И хотя в дальнейшем его действие на эту культуру становится таким же, как и у обычной воды, данное свойство такого сильно разбавленного раствора может найти применение в сельском хозяйстве, когда стоит вопрос о быстром проращивании корневой системы у протравленных зёрен, внесённых в грунт. Автор эксперимента отметил, что, во-первых, обработка протравленного зерна должна проходить непосредственно перед посевом и, во-вторых, не рекомендуется использовать раствор 1:1000 в дальнейшем при поливе, т.к. он подавляет развитие проростков.
По-видимому, в некоторых случаях сильноразбавленные растворы экзометаболитов способны конкурировать с искусственными препаратами типа «Байтан».
Влияние экзометаболитов на позвоночных животных на примере лягушки травяной изучено В.С. Геворкян (2012) Установлено, что растущие личинки (головастики) лягушки выделяют в воду экзометаболиты, подавляющие развитие более мелких особей. Автор также отметил, что экзометаболиты, достигнув в воде определённой концентрации, становятся опасными не только для мелких головастиков, но и для крупных, лидирующих в развитии, особей. Таким образом, находясь в малом объеме воды, головастики отравляют друг друга выделяемыми экзометаболитами. Отдельно (Валуев и др, 2016) исследовано влияние выделяемых озерной лягушкой Rana ridibunda пептидов на развитие корневой системы и побегов ячменя Hordeum vulgare, которые проращивали, используя растворы экзометаболитов пяти разных концентраций: от 0,01 до 100 %; контролем служила отстоявшаяся водопроводная вода. Выяснилось, что выделяемые лягушкой в состоянии покоя в зимний (неактивный) период, биологически активные вещества угнетающе воздействуют на зерно ячменя, понижая его всхожесть, развитие корневой системы и рост побегов. Однако, при увеличении светового дня и температуры окружающей среды — полученный метаболит при действии в разных концентрациях наоборот, начинает влиять на развитие ячменя уже как стимулятор.
В то же время выявлено отсутствие прямой связи между концентрацией экзометаболитов и их влиянием на растение: наиболее активно и положительно на развитие корневой системы и побегов ячменя влияет разбавленная в 10 тысяч раз исходная жидкость (Валуев и др., 2016).
Методика приготовления растворов весеннего и осеннего экзометаболитов
Пять взрослых остромордых лягушек 25 мая (весенний экзометаболит) и 5 сентября (осенний экзометаболит) были помещены в глубокий таз, с пятью литрами воды из родника. Ёмкость держали вне помещения; средняя температура окружающей среды днем: +20оС, ночью: +17оС. По истечении 5 суток из ёмкости с амфибиями взяли 1 литр жидкости, которую приняли за 100% раствор. Затем приготовили 3 раствора разной концентрации в следующей последовательности: – контроль (родниковая вода); 1:10; 1:30; 1:100. Соответствующие промеры производились по методу морфофизиологической оценки проростков, утвержденному Государственной семенной инспекцией МСХ СССР от 31.12. 1982 г.
Для эксперимента брали по 120 семян редиса сорта «Французский завтрак» с последующей закладкой на 4 полосы влажной ткани шириной 15 см, и подложкой из изолона. На ткани по заранее проведенной линии на расстоянии 2 см размещали семена зародышами вниз для удобства последующей оценки состояния проростков. Полученные 4 полосы изолона и ткани с семенами свертывали в неплотные рулоны, которые, затем, поместили в сосуды с растворами соответствующей концентрации (покрывает около 5 см нижней части рулона). Ёмкости помещали в затемнённое место на 6 суток, и в дальнейшем содержали при постоянной температуре около 20оС. Ежедневно раствор доливался до необходимого уровня. После окончания срока проращивания рулоны разворачивали, фотографировали и приступали к оценке проростков путём соответствующих промеров.
Оценка роста и развития проростков редиса была проведена нами на 4 и 6 сутки, при этом учитывались темпы роста (всхожести), количество листьев, суммарная длина стеблей, суммарная длина главного корня и боковых корешков.
Темп роста (всхожесть) рассчитывался по следующей формуле:
А=(В/С) х100%, где А – темп роста; В – число нормально развитых проростков; С – общее количество взятых для анализа семян.
Статистическая обработка полученных результатов была проведена нами на основе программы Exel 2007.
Оценка влияния различных концентраций экзометаболита
на рост и развитие проростков редиса
Через 4 суток (96 часов) всхожесть (темп роста) семян в контроле, растворах 1:10, и 1:30 была наименьшей – 30-35 мм. В то же время максимальная всхожесть (60-70 мм) наблюдалась в растворе 1:100 (весна, осень) табл. 1.
По количеству зеленых листьев в контроле (вода), растворах 1:30 и 1:10 – от 0 до 2 листьев; в 1:100 (весна, осень) 5 и 6 листьев соответственно (табл.1).
Следует отметить, что суммарная длина главного корня во всех растворах резко отличалась в сравнении с контрольным показателем. Она нарастает по мере уменьшения концентрации экзометаболита в растворах: от 105 до 249 мм в растворе 1:100 (весна) при значении 46 мм в контроле.
Сравнительный анализ результатов замера суммарной длины стеблей в каждой из групп проростков редиса показал, что они были отмечены лишь в растворе 1:100 (осень), 45 мм (табл.1).
Таблица 1
Параметры проростков семян редиса через 96 часов (4 суток)
Показатели
|
Концентрация
|
контроль
|
1:10
|
1:30
|
1:100 (весна)
|
1:100 (осень)
|
Темп всхожести (%)
|
35
|
30
|
35
|
60
|
70
|
Число семядоль-ных листьев
|
0
|
2
|
0
|
5
|
6
|
Суммарная длина главного корня, мм
|
46
|
105
|
153
|
249
|
187
|
Суммарная длина стеблей, мм
|
0
|
0
|
0
|
0
|
45
|
Аналогичные данные представлены на рис. 1, 2.
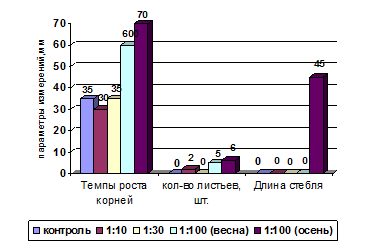
Рис.1. Параметры развития редиса через 96 часов.
Таким образом, наиболее значимым параметром развития и роста семян редиса является именно нарастание корневой системы. Чем обширнее корневая система и, соответственно, площадь питания растения, тем интенсивнее будет его рост (рис. 2).
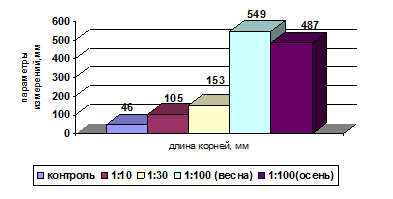
Рис.2. Параметры развития корней проростков редиса через 96 часов.
Из таблицы № 2 видно, что через 144 часа темп всхожести семян был наиболее низким в растворе метаболита 1:10 (на 5% ниже, чем в контроле). В то же время в растворе 1:30 аналогичные показатели на 10% выше контроля. Максимальные же значения влияния экзометаболита (56% выше контроля) чётко проявились как в весенних, так и осенних растворах 1:100.
Данные по количеству зеленых листьев: в контроле и 1:10 – по 5 штук, значительно большее их число отмечено во всех остальных растворах, независимо от времени получения последних (табл. 2).
Суммарная длина главного корня, формирующегося у проростков, также значительно отличается от таковых контроля (88 мм); и нарастает с уменьшением концентрации экзометаболита в растворах: от 130 мм в 1:30 до 350 мм в растворе 1:100 (осень).
Суммарная длина боковых (прилежащих) корешков во всех растворах также резко отличается от контроля; максимальная – 143 мм, в растворе 1:30, в растворах: 1:100 (74-77 мм) и в растворе 1:10 – 46 мм при значении в контроле (вода) всего 7 мм (табл. 2).
Таблица 2
Параметры развития редиса через 144 часа (6 суток)
Показатели
|
Концентрация
|
Кон-троль
|
1:10
|
1:30
|
1:100 весна
|
1:100 осень
|
Темпы всхожести
|
45
|
40
|
55
|
70
|
70
|
Число семядольных листьев, шт.
|
5
|
5
|
10
|
10
|
9
|
Общая длина боко-вых корешков, мм
|
7
|
46
|
143
|
77
|
74
|
Общая длина главного корня, мм
|
88
|
130
|
303
|
342
|
350
|
Общая длина стеблей, мм
|
78
|
105
|
258
|
291
|
255
|
Отдельно следует отметить такой показатель, как длина стеблей. Так, наиболее низкие значения выявлены в контроле (78 мм), а наибольшие – в растворе 1:100 (291 мм, весна). Аналогично высокие показатели отмечены в растворах 1:30 (258 мм), 1:100 (255мм, осень) и 1:10 (105 мм).
Обобщённые результаты эксперимента представлены на рисунках 3, 4.
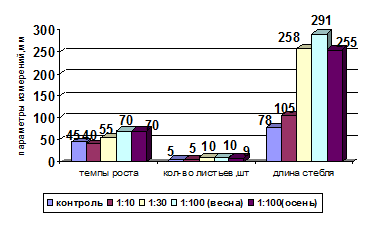
Рис. 3. Параметры развития редиса через 144 часа.
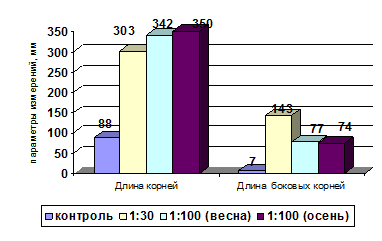
Рис.4. Параметры развития корней редиса через 144 часа.
Таким образом, экспериментально установлено положительное воздействие растворов экзометаболитов остромордой лягушки на рост и развитие проростков редиса, что позволяет сделать предварительный прогноз об аналогичном влиянии данного действующего вещества и на другие растения. Наиболее значимым фактором действия экзометаболита, стимулирующим развитие проростков является интенсивное формирование корневой системы, что необходимо растениям для устойчивого развития в период недостатка влаги.
Выявлены оптимальные показатели влияния экзометаболитов (1:100) для роста и развития проростков редиса как в весенних, так и осенних растворах, что свидетельствует об аналогичном его действии на проростки, независимо от периода активности остромордой лягушки.
Прослеживается закономерность: чем ниже концентрация раствора, тем выше положительный эффект.
Литература
Валуев В.А. Влияние экзометаболитов озёрной лягушки Rana ridibunda на обработанное 0,1% хлором зерно пшеницы // Сборник научных трудов SWorld. Материалы международной научно-практической конференции “Научные исследования и их практическое применение. Современное состояние и пути развития ‘2013”. Одесса: КУПРИЕНКО. Цит: 113-0449. Т. 38. № 1. С.38-40.
Валуев В.А. Загорская В.В., Книсс В.А., Назаров В.С., Хабибуллин В.Ф. Влияние экзометаболитов озёрной лягушки Rana ridibunda L. на развитие ячменя Hordeum vulgare (Pall.) // Экология урбанизированных территорий. 2016. № 4. С.6-11.
Геворкян В.С. Воздействие экзометаболитов на позвоночных на примере лягушки травяной Rana temporaria // Электронное научное издание Альманах Пространство и Время. 2012. Т. 1. № 1. Специальный выпуск «Система планета Земля».
Кравченко Л.В. Роль корневых экзометаболитов в интеграции микроорганизмов с растениями. Автореферат дисс. на соискание уч. степени доктора биол. наук. – Санкт-Петербург. 2000. 435 с.
Тимохина Т.Х., Марков А.А., Паромова Я.И., Самикаева В.Н., Перунова Н.Б. Способ получения экзометаболитов бифидобактерий с высокой антимикробной активностью //Медицинская наука и образованиеУрала//, Т.17, № 2 (86) Изд-во: Тюменский государственный медицинский университет (Тюмень), 2016 г. – С.152-154.
Nascimento A.C.C., Fontes W., Sebben, A., Castro M.S. Antimicrobial peptides from anurans skin secretions // Protein and Peptide Letters. 2003. 10 (3). P. 227-238.
Ponti, D., Mangoni M. L., Mignogna G., Simmaco M., Barra, D. An amphibian antimicrobial peptide variant expressed in Nicotiana tabacum confers resistance to phytopathogens // Bioch. J. 2003. Vol. 370 (1). P. 121-127.



